En esta entrada vamos a preparar
al lector para algo que llevamos tiempo prometiendo, pero que aún no hemos
hecho. FORMULACIÓN Y NOMENCLATURA DE LA QUÍMICA
ORGÁNICA. Nuestra intención es que ese hueco del blog, que pone
próximamente en descubrirlaquimica2, deje de ser un hueco y se convierta en un
espacio de información más de nuestro blog.
En esta entrada vamos a dar unas
nociones de cómo se representan las moléculas orgánicas a la hora de formular.
A diferencia de en química inorgánica no utilizamos una formula del estilo H2O,
SiH4, NH3 ¿Por qué? Esto es debido a que una fórmula
orgánica, por ejemplo, C6H12O6; puede
corresponderse con muchas estructuras moleculares, muchas moléculas, como se
muestra en la figura de debajo. Esta fórmula molecular se corresponde con
distintos azúcares. Misma fórmula molecular; distintas propiedades. Pero el
tema de la isomería y como afecta a las propiedades de las moléculas no es el
objetivo de esta entrada.
En esta imagen muestro los
azúcares en proyecciones de Fisher; en Alcanos,
alcanos ramificados y haloalcanos hablo sobre las proyecciones de Fisher y
explico cómo se llega a ellas, la idea es la misma, pero aplicándola a los
azúcares.
En entradas posteriores, hablaré
sobre los isómeros, y sobre cómo puede cambiar una molécula por “cambiar algo
de sitio”. Aunque ya en ¡El
ácido tartárico está relacionado con las tartas, no es broma! y en Carbonos
quirales y moléculas quirales, mencioné algo sobre las distintas
propiedades de los distintos isómeros.
H2O es el agua, y sólo
es agua, no hay más moléculas que se correspondan con H2O; aunque
esto también se debe a que es una molécula “pequeña”; C6H12O6
es una molécula grande y por tanto también existen varias posibilidades de
unión de los átomos. CH4 es una molécula “pequeña” y orgánica,
aunque también se estudia en química inorgánica. En este caso, solo se
representa como CH4 (es decir fórmula empírica), ya que no hay más posibilidades
de unión. Para el etano y el propano serviría usar la fórmula empírica, es
decir, C2H6 y C3H8 respectivamente.
Pero para moléculas de a partir de cuatro átomos de carbono, esto ya no
serviría, ya que C4H10 puede ser butano o 2-metilpropano.
 |
| Butano |
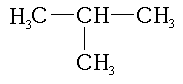 |
| 2-metilpropano |
Si esto ya ocurre con moléculas
de cinco átomos de carbono, no os quiero contar lo que ocurre con moléculas de
veinte carbonos, sobre todo cuando hay heteroátomos (carbono, nitrógeno, oxígeno),
halógenos (flúor, cloro, bromo, yodo) y dobles y triples enlaces.
Por lo que existen distintas
maneras de formular las moléculas con el fin de evitar las posibles confusiones
que surjan.
-FÓRMULA DESARROLLADA (EXPANDIDA)
Se representan todos los átomos
por sus símbolos y los enlaces que los unen por trazos.
-FÓRMULA SEMIDESARROLLADA (SEMIEXPANDIDAS O SEMICONDENSADAS)
Se omiten los trazos que
representan los enlaces entre los hidrógenos y los carbonos/heteroátomos a los
que están unidos, pero sí se indica su número empleando subíndices.
-SIMPLIFICADAS:
Se
representan las cadenas carbonadas mediante zig-zag en las que cada segmento
representa un enlace y cada punto de unión un átomo de carbono. Se omiten los átomos
de hidrógeno unidos a carbono, pero sí se incluyen los heteroátomos y sus hidrógenos.
Los dobles y triples enlaces se representan con dos y tres segmentos respectivamente.
¡OJO! LOS TRIPLES
ENLACES SE REPRESENTAN RECTOS, ES DECIR, NO SE HACE UN ZIG ZAG
Esto se debe a que, si
construimos un modelo molecular de un alquino, por ejemplo, el más sencillo que
es el etino, veremos que esa es la forma que adopta. Si hacemos esto con un
alqueno, por ejemplo, el eteno que es en este caso el alqueno más sencillo sigue
adoptando la conformación en zig-zag.
 |
| Modelo molecular del eteno |
 |
| Modelo molecular del etino |
-EN PERSPECTIVA:
Las moléculas orgánicas son
tridimensionales, por ello, aunque muchas veces representemos las moléculas en
dos dimensiones, es necesario un criterio que nos indique la orientación en el
espacio. Indicar lo que nos viene hacia nosotros, lo que está en el plano y lo
que va hacia atrás. En general representaremos con una especie de triángulo
alargado relleno o con un trazo grueso cuando queramos indicar que viene hacia
nosotros y con trazos discontinuos gordos cuando vaya hacia atrás. Esto se hace
porque los carbonos son tetraédricos, aunque no todos los carbonos son tetraédricos.
31/01/2018
Descubrirlaquimica. Estudiante de química en la USC
Descubrirlaquimica. Estudiante de química en la USC
Bibliografía:
-K.Petter C. Volhardt, Neil
E.Schore: Química orgánica estructura y función. Quinta edición. Editorial
Omega.
-E. Quiñoaa
Cabana, R. Riguera Vega: Nomenclatura y
representación de los compuestos orgánicos. Una guía de estudio y autoevaluación.
Segunda edición. Editorial McGrawHill.
-Apuntes
de las orgánicas de la carrera.











